Hľadaj
Zobraz:
Univerzity
Kategórie
Rozšírené vyhľadávanie
45 144
projektov
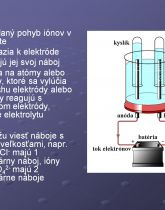
Elektrický prúd v kvapalinách
| Prípona .ppt |
Typ seminárna práca |
Stiahnuté 4 x |
| Veľkosť 0,3 MB |
Jazyk slovenský |
ID projektu 13852 |
| Posledná úprava 31.08.2021 |
Zobrazené 3 712 x |
Autor: songy |
 Zdieľaj na Facebooku
Zdieľaj na Facebooku |
||
| Detaily projektu | ||
- cena:
10 Kreditov - kvalita:
85,4% -
Stiahni
- Pridaj na porovnanie
- Univerzita:Prešovská univerzita v Prešove
- Fakulta:Fakulta humanitných a prírodných vied
- Kategória:Prírodné vedy » Fyzika
- Predmet:Fyzika
- Študijný program:-
- Ročník:2. ročník
- Formát:MS Office PowerPoint (.ppt)
- Rozsah A4:19 strán
ZÁKLADNÉ POJMY
- elektrolyty → roztoky kyselín (napr. H2SO4, HNO3) , zásad (napr. KOH, NaOH) a solí (napr. NaCl, KCl) , ktoré vedú elektrický prúd
- vodivosť elektrolytov spôsobujú voľne pohyblivé kladne a záporne nabité ióny - katióny a anióny, uvádzané do pohybu elektrickým poľom, ktoré vzniká medzi elektródami ponorenými do elektrolytu
- elektróda → časť vodiča, ktorou sa privádza elektrický prúd do danej sústavy (napr. roztoku elektrolytu, plynu, vákua, tuhej látky). - anóda (elektróda zapojená na kladnú svorku zdroja) - katóda (elektróda zapojená na zápornú svorku zdroja)
- elektrolytická disociácia → dej, pri ktorom vznikajú voľné ióny rozpadom rozpustnej látky v rozpúšťadle
ELEKTROLÝZA
- je jav, keď pri prechode elek. prúdu elektrolytom nastávajú na elektródach látkové zmeny
- pri elektrolýze sa na katóde vždy vylučuje vodík alebo kov
- využitie: elektrometalurgia, galvanické pokovovanie (galvanostégia), galvanické leptanie, galvanoplastika, polarografia, výroba niektorých kovov (napr. hliník z Al2O3)
...
- elektrolyty → roztoky kyselín (napr. H2SO4, HNO3) , zásad (napr. KOH, NaOH) a solí (napr. NaCl, KCl) , ktoré vedú elektrický prúd
- vodivosť elektrolytov spôsobujú voľne pohyblivé kladne a záporne nabité ióny - katióny a anióny, uvádzané do pohybu elektrickým poľom, ktoré vzniká medzi elektródami ponorenými do elektrolytu
- elektróda → časť vodiča, ktorou sa privádza elektrický prúd do danej sústavy (napr. roztoku elektrolytu, plynu, vákua, tuhej látky). - anóda (elektróda zapojená na kladnú svorku zdroja) - katóda (elektróda zapojená na zápornú svorku zdroja)
- elektrolytická disociácia → dej, pri ktorom vznikajú voľné ióny rozpadom rozpustnej látky v rozpúšťadle
ELEKTROLÝZA
- je jav, keď pri prechode elek. prúdu elektrolytom nastávajú na elektródach látkové zmeny
- pri elektrolýze sa na katóde vždy vylučuje vodík alebo kov
- využitie: elektrometalurgia, galvanické pokovovanie (galvanostégia), galvanické leptanie, galvanoplastika, polarografia, výroba niektorých kovov (napr. hliník z Al2O3)
...
Kľúčové slová:
elektrolyty
ióny
katióny
anióny
elektrolýza
korózia
faradayové zákony pre elektrolýzu
galvanický článok
primárny článok
sekundárny článok
akumulátor
suchý článok
alkalický článok
Obsah:
- ZÁKLADNÉ POJMY
ELEKTROLÝZA
KORÓZIA
FARADAYOVE ZÁKONY PRE ELEKTROLÝZU
GALVANICKÉ ČLÁNKY
PREHĽAD ELEKTROCHEMICKÝCH ČLÁNKOV
DANIELLOV ČLÁNOK
Zdroje:
- skriptá
- poznámky
- internet